
责编丨迦溆
铁死亡(Ferroptosis)是最近发现的由铁依赖性脂质过氧化驱动的调节性细胞死亡形式(regulated cell death, or RCD),在形态学和机制上不同于其他RCD。机制上,细胞膜中的含多不饱和脂肪酸的磷脂(polyunsaturated-fatty-acid–containing phospholipids, or PUFA-PLs)在富含铁和活性氧(reactive oxygen species, or ROS)的条件下易发生过氧化,这种脂质过氧化物在细胞膜中的积累最终会破坏膜的完整性,从而导致铁死亡。近来研究表明,铁死亡在肿瘤抑制以及某些癌症治疗中起着重要作用,而靶向铁死亡已成为一种有前途的癌症治疗策略。
#放疗#(radiotherapy or RT)是癌症治疗的基石,它通过靶向递送电离辐射(ionizing radiation or IR)来消灭癌细胞。IR可以直接诱导各种类型的DNA损伤,还可引发细胞水的辐射分解并刺激氧化酶产生高反应性的活性氧来损害核酸,脂质和蛋白质。这些直接和间接作用共同杀伤癌细胞,包括诱导细胞周期停滞,衰老和凋亡。然而,其他形式的RCD在放疗中的潜在作用有待进一步研究。

2021年4月23日,美国MD安德森癌症中心甘波谊团队在Protein & Cell杂志上发表了名为Ferroptosis, radiotherapy, and combination therapeutic strategies的综述,总结了放疗与铁死亡之间相互影响的机制,讨论了铁死亡与放疗诱导的其他RCD之间的相互作用,并探讨了放疗和免疫疗法中靶向铁死亡的联合治疗策略。

1. 放疗诱导的细胞效应
放疗诱导DNA损伤后, ATM和ATR迅速检测到这些损伤,诱导复杂的信号级联反应(DNA damage response or DDR),激活下游的检查点激酶1 / 2(CHEK1 / 2)等使细胞周期阻滞,促进损伤的 DNA修复;若存在无法修复的DNA损伤,细胞则启动凋亡程序。p53在放疗诱导的细胞效应中起重要作用,调控放疗后细胞的衰老和凋亡。此外,放疗还可以诱导自噬,坏死性凋亡以及有丝分裂灾难,而放疗诱导的细胞坏死被认为是一些放疗副作用的原因,例如脑或肺部放射性坏死。总之,放疗可以诱导复杂的下游信号途径,引发多种细胞效应。
2. 铁死亡的调控网络以及诱导剂
铁死亡的调控主要是铁死亡防御系统和铁死亡执行系统的博弈(下图1)。铁死亡防御系统主要包括GPX4依赖的系统(SLC7A11-GSH-GPX4轴)和GPX4非依赖的系统(如NAD(P)H-FSP1-CoQ轴和DHFR-BH4-GCH1轴)。铁死亡执行系统包括PUFA-PL的合成和过氧化,以及铁代谢。由LPCAT3和ACSL4介导的PUFA-PL合成,以及ALOXs和POR介导的PUFA-PL过氧化是铁死亡发生的必要条件。细胞内的不稳定铁(Fe2+)可通过Fenton反应产生大量ROS,为脂质过氧化提供触充分的原料,并且其也是脂质过氧化酶(ALOXs和POR)的辅因子,决定了这些酶的活性。
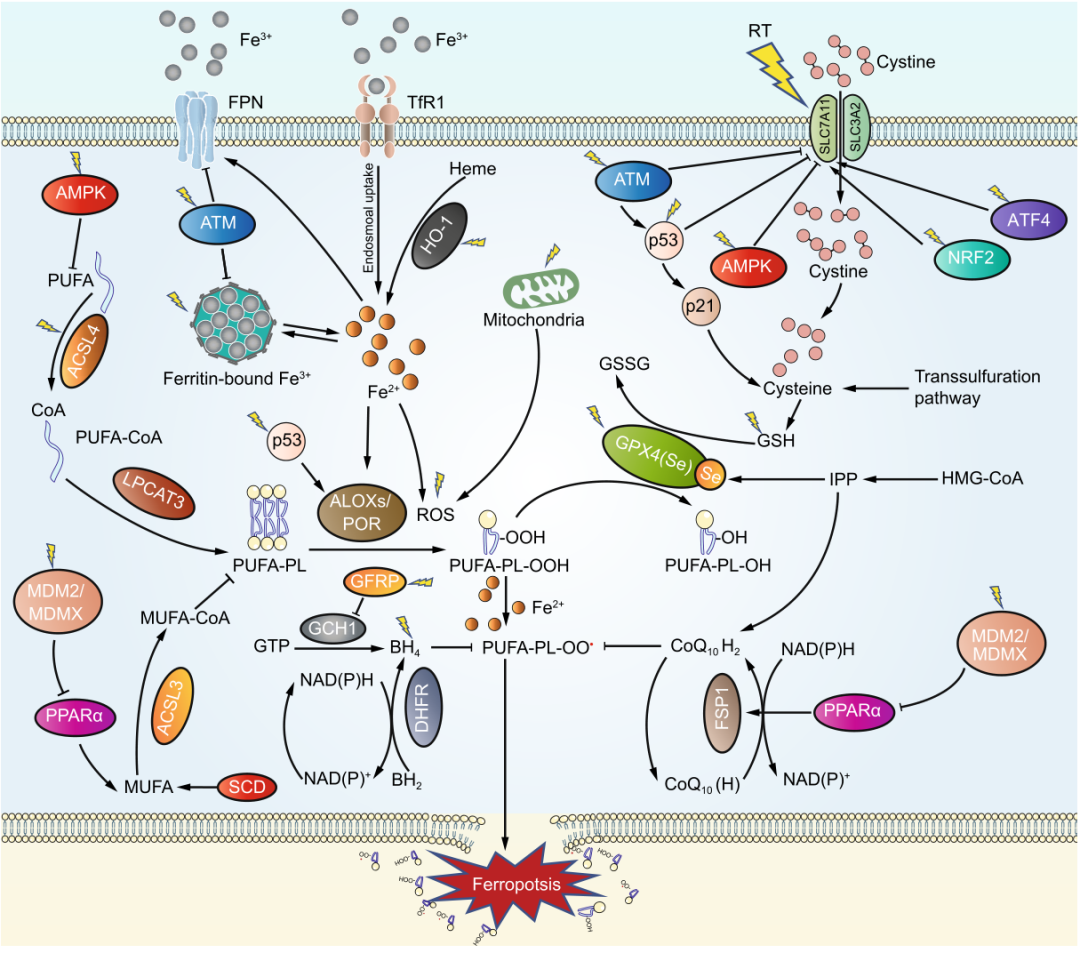
目前已经发现了几类铁死亡诱导剂(FIN),包括抑制SLC7A11活性或消耗GSH的I类FIN,抑制GPX4活性的II类FIN,消耗CoQ和GPX4的III类FIN,以及其他类型的FIN。此外,一些纳米材料也可以在肿瘤局部诱导铁死亡。这些FIN在癌症治疗中可能起到重要作用。
3. 放疗和铁死亡
最近的研究在多种肿瘤中发现了大量的遗传和生化证据,表明放疗与铁死亡之间存在紧密联系。首先,放疗能够促进脂质过氧化,并诱导铁死亡标志基因PTGS2的表达;此外,放疗后的肿瘤细胞出现了典型的铁死亡形态学特征:线粒体收缩和膜密度增加;最后,用铁死亡抑制剂可以部分恢复放疗后细胞的存活,其恢复效果甚至强于其他RCD抑制剂。值得注意地,不同的放疗剂量和分割模式也会对铁死亡的诱导程度产生影响。
机制上,放疗可能通过至少三个平行途径诱导脂质过氧化和铁死亡(下图2)。首先,放疗可以通过产生过量的ROS来诱导脂质过氧化;此外,IR上调ACSL4的表达以促进PUFA-PLs的生物合成;最后,放疗还导致GSH耗竭,这削弱了GPX4介导的铁死亡防御能力,并进一步促进了放疗诱导的铁死亡。一项研究表明,放疗以ATM依赖性方式抑制SLC7A11的表达,并认为放疗介导的SLC7A11抑制可通过减少胱氨酸摄取和GSH合成来触发铁死亡。然而,其他研究表明,SLC7A11的表达可被放疗诱导,这可能是一种适应性反应以保护细胞免受铁死亡,其可能涉及NRF2和/或ATF4,它们通常都被放疗激活并可调节SLC7A11的转录。因此,放疗对SLC7A11的调控似乎是背景依赖性的,例如细胞系,放疗剂量或持续时间。
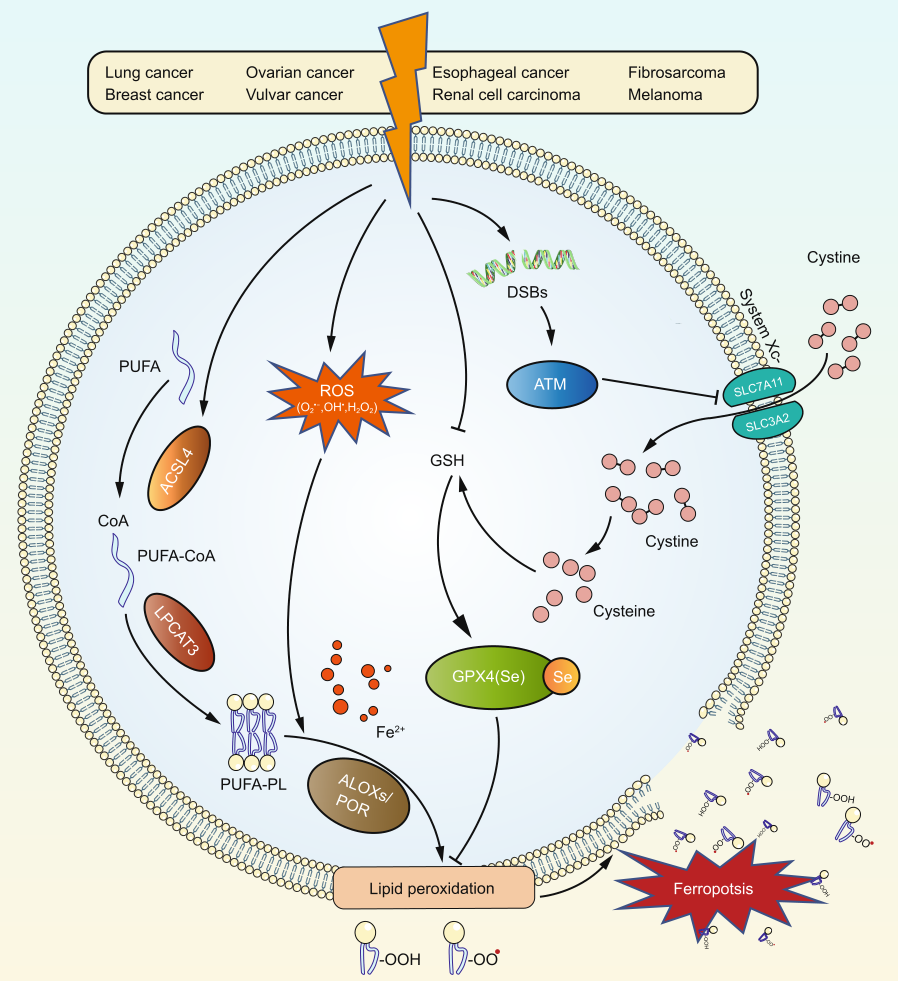
此外,由于多种代谢途径参与了铁死亡调控,并且其中一些基因也受放疗调控,因此其他潜在机制也可能有助于放疗诱导的铁死亡(图1),如p53,AMPK,MDM2和GCH1-BH 4信号轴。放疗还可以诱导HO-1和FTH1的表达以影响铁代谢,并且线粒体也可能参与了放疗诱导的铁死亡。总之, 放疗引起的铁死亡可能涉及多种机制,需要进一步的研究来全面理解放疗诱导的铁死亡。
铁死亡与放疗诱导的其他细胞效应之间也存在一些重要交联(下图3)。放疗诱导DNA损伤从而激活ATM,p53或RB,这可能与放疗诱导的免疫原性细胞死亡(ICD)有关,例如细胞凋亡,坏死性凋亡和自噬。这些ICD与放疗诱导的衰老相关的分泌表型(SASP)一起激活T细胞并将其募集到肿瘤部位,而CD8 + T细胞分泌的IFNγ进一步促进放疗诱导的铁死亡。此外,放疗诱导的自噬也可以促进铁死亡,并且在分子水平上,放疗诱导的DNA损伤似乎通过多种机制同时介导铁死亡和其他RCD。进一步理解铁死亡和其他细胞效应之间的相互作用,可以提供对放射抵抗机制和放射增敏策略的新见解。
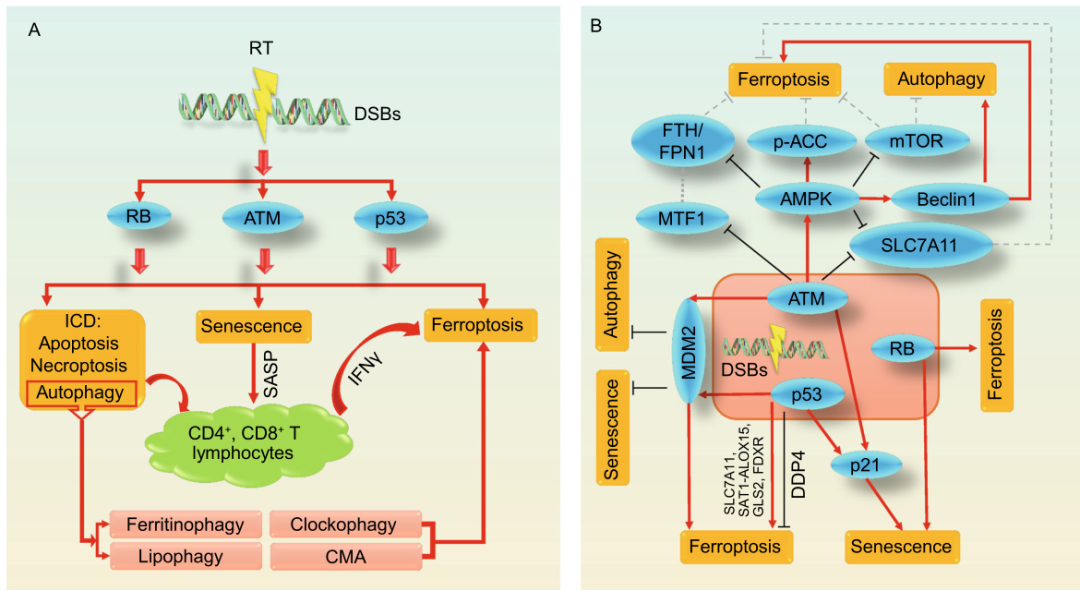
4. 铁死亡在放射增敏中的作用
铁死亡在肿瘤的放射敏感性中起重要作用(下图4)。肿瘤细胞可以上调SLC7A11和GPX4以保护细胞免受放疗诱导的铁死亡,并且在KEAP1突变肿瘤中通过上调SLC7A11,抑制铁死亡并导致放射抵抗。因此,靶向抑制SLC7A11或者GPX4可以增敏放疗。此外,抑制PUFA-PLs的合成(如ACSL4失活)可抑制放疗诱导的铁死亡,导致放射抵抗;而补充PUFA-PLs(如通过纳米材料)或者减少MUFA-PLs的合成(如ACSL3失活)可促进放疗诱导的铁死亡并增敏放疗。
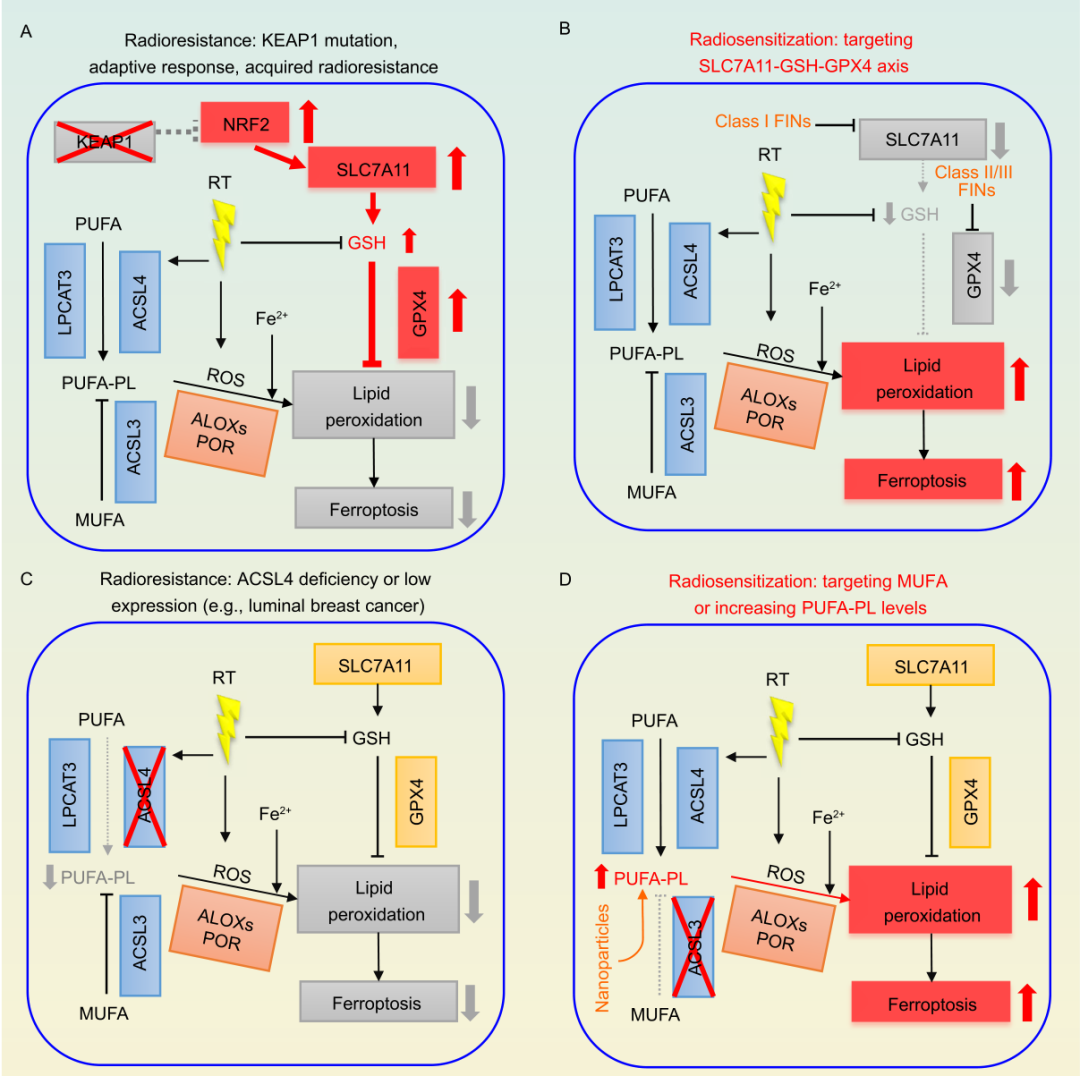
肿瘤乏氧是放射抵抗重要的机制(下图5)。但低氧环境可以促进肿瘤细胞产生ROS,并激活HIFs-HILPDA轴以促进PUFA-PLs的形成,这使得乏氧肿瘤细胞对铁死亡敏感。因此,放疗联合FIN是克服肿瘤乏氧导致的放射抵抗的潜在策略。
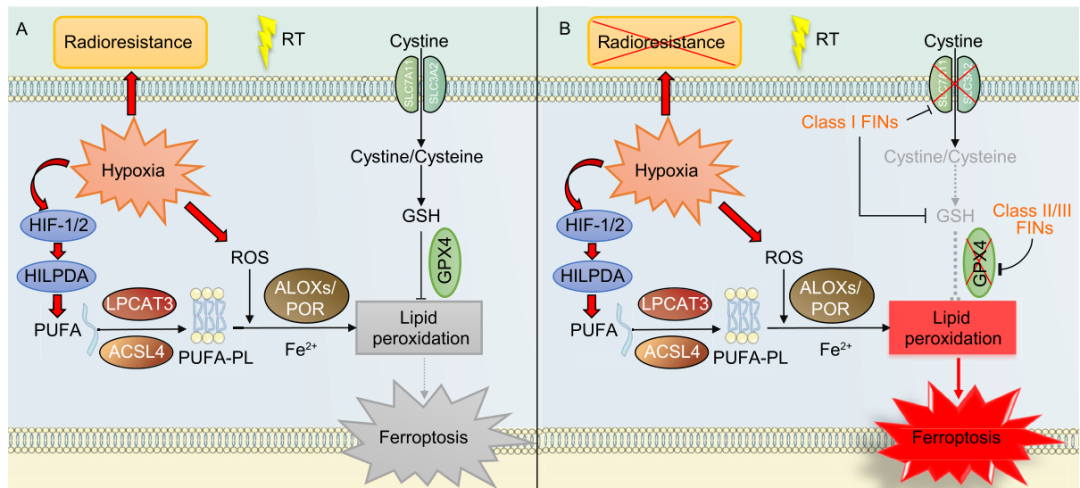
放疗与靶向SLC7A11的FIN(例如柳氮磺吡啶,IKE,索拉非尼)在体内联合中显示出了强协同性和良好的安全性。抑制GSH合成(例如BSO)或靶向GPX4的FIN在体外也可有效增敏放疗。虽然经典的GPX4抑制剂(例如RSL3和ML162)不适合在体内使用,但具有抑制GPX4功能的withaferin A和altretamine(经FDA批准的化疗药)在体内显示出良好的抗肿瘤活性,是体内靶向GPX4的潜在选择。然而,仍需要进一步的研究来确定GPX4抑制剂在癌症治疗中的治疗窗口,并探索在肿瘤中局部靶向GPX4进行放射增敏的技术。
免疫系统激活是放疗介导的抗癌作用中不可或缺的一部分。铁死亡最近被发现是免疫治疗和放疗之间的交联点。CD8 + T细胞分泌的IFNγ和放疗激活的ATM可以协同抑制SLC7A11表达,促进脂质过氧化和铁死亡。抑制铁死亡可以削弱免疫检查点抑制剂(ICI)联合放疗的疗效,而灭活肿瘤中的SLC7A11可以进一步增强ICI和放疗的协同作用。
值得注意地是,需要识别特定生物标记物以预测肿瘤对放疗联合ICI的敏感性。肿瘤具有铁死亡抑制基因低表达和/或铁死亡促进基因高表达的特征,可能是适合放疗联合ICI治疗的指征。对于那些铁死亡诱导不足的肿瘤,将FINs与ICI和放疗结合以恢复肿瘤铁死亡可能是有希望的联合治疗策略。
结论和未来展望
最近的研究确立了铁死亡在放疗中的关键作用,并进一步表明在放疗以及联合免疫治疗中靶向铁死亡是有希望的联合治疗策略。同时,作者对放疗与铁死亡的未来研究方向,提出以下几点建议。
1. 不同类型的癌症之间的放射敏感性存在显着差异。即使在相同的肿瘤类型中,由于肿瘤的异质性,个体之间的放射敏感性也可能有很大差异。因此,为个体化放疗确定合适的生物标志物至关重要。研究表明,与放疗前匹配的肿瘤样本相比,放疗后患者的肿瘤样本中发现了铁死亡标记物4-HNE水平升高,并且其升高程度与放疗反应正相关。因此,进一步剖析放疗和铁死亡之间的相互作用,并基于此探索用于患者分层的生物标记物,可能有助于识别放射敏感的个体,以及明确适合放疗联合FIN治疗的人群。
2. 尽管FIN 联合放疗在临床前研究中似乎是安全的,但铁死亡也可能与放疗诱导的正常组织损伤有关。进一步阐明放疗与FIN联合使用是否对正常组织的毒性要小于肿瘤(即是否存在最佳治疗窗口)至关重要。具有FIN活性的纳米材料的研发可能是解决此问题的另一种方法。
3. 目前有关铁死亡在放疗中的研究主要集中在X射线(一种低LET的光子),而质子和其他高LET辐射(如碳离子)在放疗中的应用也不断发展,其中一些已证明比光子疗法具有更好的疗效。因此,探索铁死亡在质子和其他高LET辐射中的潜在作用将是有趣的方向。
原文链接:
https://link.springer.com/article/10.1007/s13238-021-00841-y
通讯作者介绍:

论文通讯作者甘波谊教授任职于美国德克萨斯大学MD安德森癌症中心放射肿瘤学系,长期从事肿瘤代谢、铁死亡、肿瘤治疗等方向研究,在Nature、Cancer Cell、Nature Cell Biology、Nature Communications、PNAS、Cell Research、Cancer Research等杂志发表文章60多篇,引用超过13,000次。主持NIH、CPRIT等机构的多个研究项目,担任众多国际知名学术期刊评委。值得一提的是, 甘波谊教授团队近年在国际知名杂志, 如 Nature Cell Biology, Cell Research, Nature Communications, 已经发表多篇论文阐述铁死亡和胱氨酸代谢与肿瘤发生及治疗的关系。

