
责编丨迦溆
#肿瘤#
代谢重编程与表观遗传学改变是肿瘤的两大重要特征。近年来的研究表明,二者之间存在非常广泛的相互调控关系。一方面,癌症特征性的代谢改变、肿瘤微环境因素和饮食干预等会通过改变代谢物水平影响表观遗传修饰酶及辅因子的活性或底物丰度,从而参与表观遗传学调控;另一方面,表观遗传修饰酶的表达或活性改变也会对细胞的代谢产生广泛的直接或间接的影响。因此,全面理解肿瘤发生发展过程中机体的代谢及表观遗传修饰的特征性改变,系统总结代谢与表观遗传的过去发现、当前趋势以及未来研究方向,将有助于开发针对肿瘤代谢-表观遗传特征性改变的新的联合治疗策略和思路。

2021年5月29日,华南理工大学的孙林冲、高平教授和中国科学技术大学的张华凤教授在Protein & Cell发表了题为Metabolic reprogramming and epigenetic modifications on the path to cancer的综述长文。该论文全面概括了肿瘤进程中整合代谢与表观遗传修饰的分子通路,详细阐述了代谢改变在乙酰化(acetylation)、甲基化(metylation)、琥珀酰化(succinylation)、β-羟基丁酰化(β-hydroxybutyrylation)、乳酰化(lactylation)等重要表观遗传修饰中的作用和机制,并系统总结了近年来从靶向代谢相关的染色质修饰以及饮食干预的角度治疗肿瘤的最新进展、潜在策略以及应用前景。

一、肿瘤发展过程中代谢和表观遗传修饰的整合
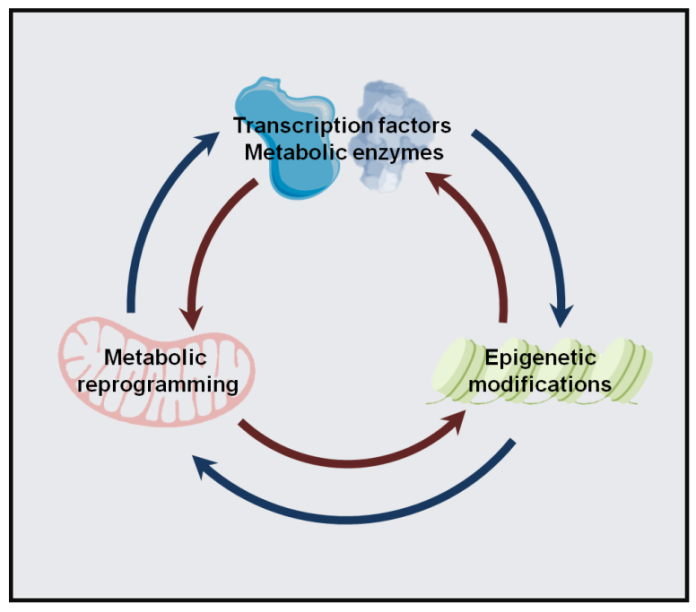
长期以来,肿瘤被认为是一种由癌基因和抑癌基因突变驱动的遗传性疾病。然而在过去的三十多年里,随着高通量测序等新兴技术的快速发展,表观遗传变化被越来越多地认为是另一个主要的致癌因素。表观遗传修饰是调节基因表达而不改变DNA序列本身的过程。癌症中的表观遗传失调通常包括表观遗传修饰酶的突变和/或异常表达以及相关辅因子水平的改变,它们通过改变染色质的结构和动力学从而导致基因表达的改变,最终促进肿瘤的发生和进化。与此同时,越来越多的研究表明代谢重编程通过产生额外的能量、提供更多的生物大分子用于细胞生物合成的同时,还可通过平衡肿瘤细胞中的氧化还原状态促进肿瘤的发生发展。癌基因和抑癌基因的突变可以驱动代谢和表观遗传修饰的重塑,同时它们也受到表观遗传修饰及代谢物水平改变的调节(图1)。然而,我们对于肿瘤中癌基因/抑癌基因的紊乱、代谢重编程以及表观遗传修饰之间的紧密地交织以及它们的异常串扰如何影响肿瘤还缺乏全面的理解。因此,进一步阐明它们之间的联系对于更有效的肿瘤治疗是必要且迫切的。
二、代谢产物在肿瘤表观遗传重塑中发挥着关键作用
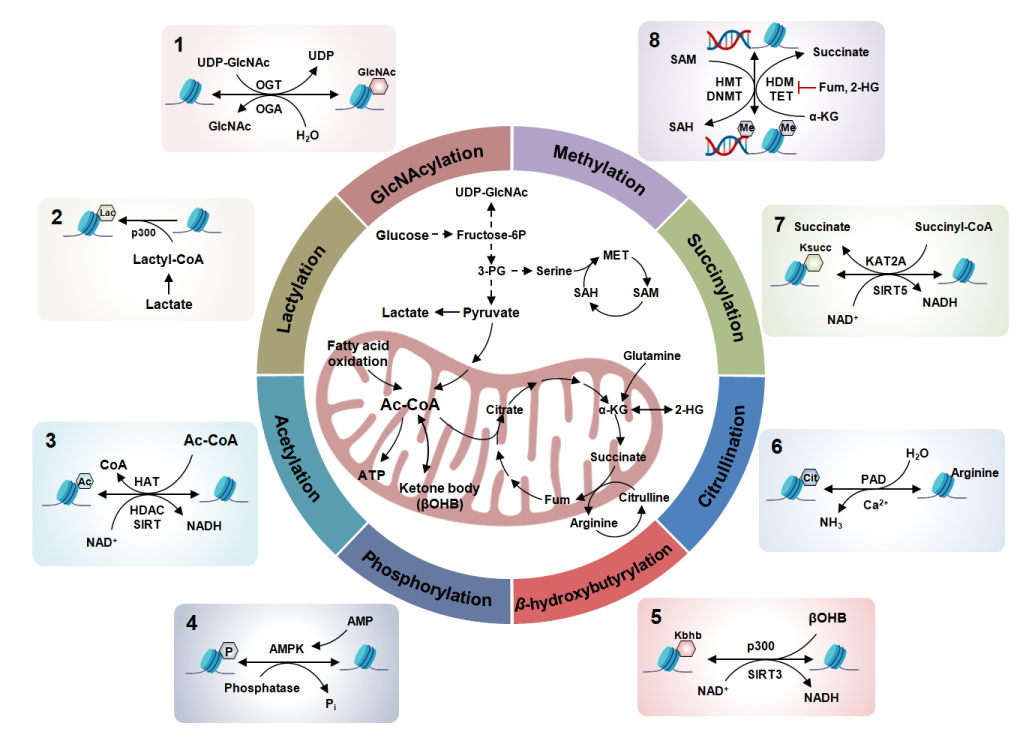
几乎所有的表观遗传修饰过程均需要代谢物的参与,例如乙酰辅酶A(acetyl-CoA), 烟酰胺腺嘌呤二核苷酸(nicotinamide adenine dinucleotide/NAD+),S-腺苷甲硫胺酸(S-adenosyl methionine/SAM),α-酮戊二酸(α-ketoglutarate/α-KG),黄素腺嘌呤二核苷酸(flavin adenine dinucleotide/FAD),腺苷三磷酸(adenosine triphosphate/ATP)和琥珀酸(succinate)等作为底物或辅因子等参与乙酰化、甲基化、磷酸化、琥珀酰化等翻译后修饰过程(图2)。因此,代谢产物在肿瘤表观遗传修饰中发挥着非常广泛而重要的作用。
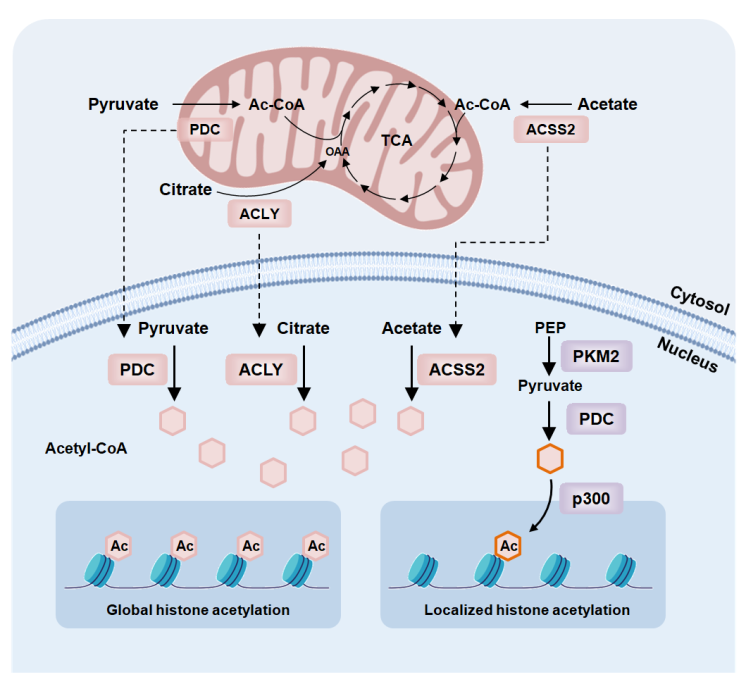
Acetyl-CoA和NAD+是参与(组)蛋白乙酰化修饰的主要代谢物。在大多数哺乳动物细胞中,acetyl-CoA主要是由线粒体中的丙酮酸脱氢酶复合物(PDC)将葡萄糖来源的丙酮酸(pyruvate)进一步反应生成的中心代谢物。脂肪酸β-氧化(β-oxidation)、支链氨基酸(BCAA)分解代谢和游离的乙酸(acetate)都有助于线粒体acetyl-CoA的生成。由于线粒体膜上并不存在acetyl-CoA转运蛋白,因此线粒体中生成的acetyl-CoA并不能在细胞器中自由穿梭。肿瘤微环境中的肿瘤细胞则巧妙的通过将PDC复合物易位至细胞核中完成acetyl-CoA的生成,参与核心组蛋白H2B,H3,H4的乙酰化修饰,通过促进固醇调控元件结合转录因子(SREBF)调节脂代谢酶、胆固醇代谢酶的表达等促进肿瘤发展或转移。定位于细胞质的ATP柠檬酸裂解酶(ACLY)也被发现在细胞核中存在,而且核定位的ACLY是组蛋白乙酰化和同源重组介导的DNA修复所需acetyl-CoA的主要来源。在免疫微环境中,ACLY通过乙酰化修饰M2型(M2 macrophages)基因的表达在巨噬细胞的活化和极化中发挥重要作用;而且有研究表明ACLY激活及其介导的乙酰化修饰对T细胞的增殖至关重要。快速增殖、低氧或脂缺乏条件下的肿瘤细胞,则可诱导细胞质定位的乙酰辅酶A合成酶2(ACSS2)的高表达,通过吸收、利用乙酸为细胞提供acetyl-CoA。核定位的ACSS2通过维持组蛋白乙酰化水平参与脂代谢基因的表达(图3)。NAD+是赖氨酸残基去乙酰化过程中去乙酰化酶sirtuins的辅助因子,NAD+/NADH比值与肿瘤细胞的乙酰化状态和能量状态密切相关。此外,蛋白的乙酰化修饰可调控转录因子和代谢酶的定位、活性和功能,如:SIRT1通过去乙酰化低氧诱导因子1(HIF-1)降低其稳定性,从而抑制肿瘤生长和血管新生;磷酸甘油醛脱氢酶(GAPDH)和丙酮酸激酶(PKM2)的乙酰化修饰在改变这些代谢酶活性的同时也可促进其向细胞核易位,从而参与肿瘤细胞生长以及肿瘤发生等。
代谢调控(组)蛋白和DNA甲基化。组蛋白甲基转移酶(histone methyltransferases /HMTs)和DNA甲基转移酶(DNA methyltransferases/DNMTs)均需要SAM(由甲硫氨酸、苏氨酸、丝氨酸等一碳代谢相关氨基酸衍生)作为组蛋白和DNA的甲基供体(图2)。甲硫氨酸循环中产生的SAM是组蛋白或DNA甲基化的主要甲基供体,在正常小鼠及人源的肿瘤细胞中,甲硫氨酸代谢均可通过动态调节H3K4me3的三甲基化来调控基因组结构、染色质动态和基因表达。肿瘤细胞通过甲硫氨酸转运体SLC3A2可以从肿瘤微环境中吸收并利用大量甲硫氨酸,导致T细胞内甲硫氨酸利用的缺乏以及随后T细胞内H3K79me2的缺失,最终肿瘤细胞通过在表观遗传水平损害T细胞的杀伤功能启动免疫逃逸。丝氨酸和甘氨酸通过提供β碳原子进入叶酸循环(folate cycle)从而整合入甲硫氨酸循环。近期的研究表明,磷酸丝氨酸转氨酶1(PSAT1)在LKB1缺失或KRAS活化条件下的激活以及丝氨酸羟甲基转移酶(SHMT2)的自身扩增均可通过DNA甲基化参与胰腺癌或B淋巴瘤。亚铁和α-KG是去甲基转移酶(histone demethylases/HDMs,ten-eleven translocation enzymes/TETs等)的必备底物及辅因子。此外,三羧酸循环中的其它中间产物,如2-羟戊二酸(2-HG)、琥珀酸和富马酸(fumarate)等与α-KG结构相似,通过竞争拮抗α-KG的功能抑制去甲基转移酶的活性参与组蛋白和DNA的甲基化调控。例如:异柠檬酸脱氢酶(IDH)的突变会导致2-HG的累积,白血病患者IDH1和IDH2突变通过破坏TET2功能诱导整体DNA高甲基化,损害造血分化,最终促进恶性转化。此外,这些中间产物还可通过抑制双加氧酶如PHD的活性影响HIF信号通路,调节T细胞的组蛋白甲基化水平以及DNA修复等广泛参与不同类型肿瘤的发生和发展。
琥珀酰辅酶A(succinyl-coA)和(组)蛋白琥珀酰化。三羧酸环衍生的琥珀酰辅酶A是琥珀酰化的主要底物。琥珀酰辅酶A可由三羧酸循环、脂质和氨基酸代谢(组氨酸、脯氨酸、谷氨酰胺等)产生(图2)。线粒体中琥珀酸脱氢酶(succinate dehydrogenase/SDH)的缺失或突变导致的琥珀酰辅酶A累积以及去琥珀酰化酶SIRT5的敲除,均会诱导组蛋白高琥珀酰化以及致癌性的代谢改变和肿瘤细胞的凋亡抵抗。新近的研究表明α-酮戊二酸脱氢酶(α-ketoglutarate Dehydrogenase/α-KGDH)通过结合组蛋白乙酰转移酶KAT2A形成复合物发挥琥珀酰转移酶的功能,通过琥珀酰化组蛋白H3K79促进脑瘤的生长。谷氨酸脱氢酶(GDH)、苹果酸脱氢酶(MDH)、柠檬酸合酶(CS)、PKM2等代谢酶均可受到琥珀酰化修饰的调控,最终通过影响这些代谢酶的活性或功能参与肿瘤调节或肿瘤免疫。
酮体代谢与β-羟基丁酰化(β-hydroxybutyrylation)。酮体主要由丙酮、乙酸和β-羟基丁酸等三大类脂类代谢产物组成。机体在葡萄糖缺乏情况下,肝脏产生的β-羟基丁酸可作为多种组织的替代能源。越来越多的证据表明,β-羟基丁酸还具有能量供应以外的功能,例如参与翻译后修饰(图2)。酰基转移酶p300可以介导组蛋白β-羟基丁酰化,SIRT3则可以选择性地去除β-羟基丁酰化。β-OHB通过上调Foxo1和Ppargc1a等转录因子的H3K9bhb参与CD8+ Tmem细胞的记忆形成。抑癌蛋白p53经过β-羟基丁酰化修饰以后,可通过抑制其自身的乙酰化及靶基因p21等的表达,促进肿瘤细胞的增殖。
乳酸与乳酰化修饰。乳酸长期以来被认为是一种代谢废物,但是近年来的研究表明它不仅可以被肿瘤组织再利用提供能量以外,还可作为底物修饰组蛋白赖氨酸残基,称之为乳酰化修饰(图2)。在人类HeLa细胞和小鼠骨髓来源的巨噬细胞(BMDMs)中的核心组蛋白如H3、H4、H2A和H2B上鉴定出28个赖氨酸乳酰化(Kla)位点。在低氧或巨噬细胞向M1型极化等会导致乳酸增多的条件下,细胞内的组蛋白乳酰化水平明显升高并促进相关基因的转录及表达。从小鼠的黑色素瘤及肺癌组织中分离得到的致癌型的M2型巨噬细胞与乳酰化水平显著正相关,暗示巨噬细胞中高乳酸和高组蛋白乳酰化水平可能有助于肿瘤的形成和恶性进展。
磷酸化(phosphorylation)、糖基化(O-GlcNAcylation)、瓜氨酸化(citrullination)以及衣康酰化(itaconation)。除赖氨酸可被广泛的进行酰化修饰以外,丝氨酸和苏氨酸可被广泛的进行磷酸化和糖基化修饰(图2)。ATP介导的组蛋白磷酸化与肿瘤细胞的多种生物学过程有关,如转录激活、有丝分裂、减数分裂、DNA修复和凋亡等。二磷酸尿苷N-乙酰葡糖胺(uridine diphosphate GlcNAc/UDP-GlcNAc)是融合葡萄糖、谷氨酰胺、氨基酸、脂肪酸和核苷酸代谢的己糖胺生物合成途径(HBP)的最终产物,是糖基化修饰的直接供体和底物(图2)。糖基化修饰调控基本如转录、表观遗传编程和细胞信号通路激活等细胞生物学过程;因此,其破坏与多种肿瘤的病理过程有关。组蛋白瓜氨酸化影响约10%的组蛋白分子,这种较少受到关注的翻译后修饰通过肽酰精氨酸脱亚胺酶(PAD或PADI)将精氨酸残基转化为瓜氨酸,导致氢键减少以及染色质结构的松散(图2)。在不同类型的晚期癌症患者中,组蛋白H3的瓜氨酸化修饰增强并参与中性粒细胞胞外陷阱(neutrophil extracellular traps/NETs)的形成。衣康酸是新近在巨噬细胞中发现的发挥显著抗炎作用的代谢物,与神经胶质瘤及腹膜肿瘤(B16黑色素瘤和ID8卵巢癌)生长显著相关。衣康酸被发现可通过烷基化修饰半胱氨酸残基修饰KEAP1、谷胱甘肽(GSH),NLRP3,ALDOA,GAPDH,LDHA,以及其他涉及炎症小体、Toll样信号、细胞死亡和DNA损伤的相关蛋白。但目前尚不清楚衣康酸是否直接通过衣康酰化,衣康酰辅酶A(itaconyl-CoA),或间接通过衣康酸相关的其他代谢物影响免疫细胞或肿瘤细胞的表观遗传重塑以及肿瘤发生和发展。
三、靶向与代谢相关的染色质修饰治疗肿瘤
靶向乙酰化治疗肿瘤。近几十年来,以组蛋白或DNA的表观遗传调控为靶点来实现肿瘤治疗引起了越来越多的关注。研究最广泛的表观遗传抑制剂是组蛋白去乙酰化酶(histone deacetylase/HDAC)抑制剂。HDAC抑制剂通过抑制HDACs活性增强组蛋白或非组蛋白赖氨酸残基的乙酰化修饰水平,从而诱导细胞死亡、细胞周期阻滞、衰老、分化、自噬和肿瘤免疫原性等达到抑制肿瘤的目的。基于靶向ACLY,ACSS2,PDK等代谢-表观遗传互作的抑制剂如SB-204990,ETC-1002,DCA等也正在进行临床前或临床试验。
靶向甲基化治疗肿瘤。肿瘤抑制基因的频繁高甲基化促进肿瘤的发展,因此通过阻断DNMTs来去甲基化DNA是一种潜在的治疗策略。阿扎胞苷(azacitidine)和地西他滨(decitabine)是最古老的DNMTs抑制剂,被FDA批准用于治疗慢性骨髓单核细胞白血病(chronic myelomonocytic leukemia)和一系列其他类型的恶性肿瘤。它们是核苷类似物,在细胞周期的S期与DNA结合并与DNMTs形成不可逆的复合物,导致DNMTs的降解。与乙酰化和DNA甲基化抑制剂相比,组蛋白甲基化相关的抑制剂较少。由于IDH突变通过广泛抑制组蛋白去甲基化酶HDMs活性导致整个基因组的组蛋白高甲基化,因此目前以代谢酶IDH突变为靶点治疗脑胶质瘤和急性髓性白血病已经成为一种可期的肿瘤治疗手段。
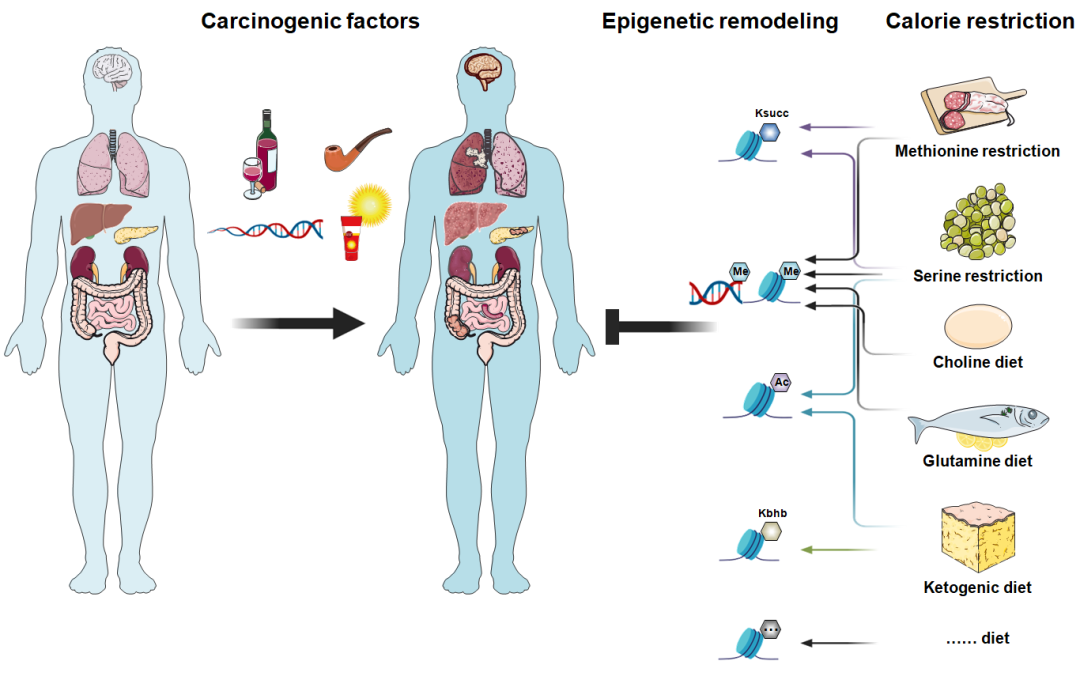
以表观遗传修饰酶和代谢分子为靶点的膳食干预治疗肿瘤。热量限制和禁食已被证明可以延长寿命,促进机体健康,因此膳食干预近年来逐渐成为很有前途的抗肿瘤疗法。越来越多的研究发现饮食中甲硫氨酸、丝氨酸和甘氨酸、酮体、胆碱、精氨酸、谷氨酰胺、果糖、半胱氨酸等营养物质的改变通过影响表观遗传修饰水平参与不同类型肿瘤的发生(图4)。例如:高脂肪、低碳水化合物的生酮饮食可以抑制肿瘤的发展,而高脂肪、高碳水化合物的饮食则会导致肥胖促进肿瘤的发展;甲硫氨酸限制的饮食可以抑制肿瘤的侵袭和转移;丝氨酸和甘氨酸限制的饮食减缓肿瘤生长,提高小鼠的存活率等;此外,与我们的理解相悖的是,有研究表明体内谷氨酰胺来源的α-KG通过促进H3K4me3的低甲基化,从而抑制黑色素瘤中表观遗传改变所激活的致癌性信号通路。总体而言,目前关于饮食干预治疗肿瘤过程中的表观遗传变化及其与肿瘤进程的关系的相关证据还极其缺乏,尽管科学家们在动物实验中获得了令人满意的结果,但在进入临床阶段之前,还需要进行大量的深入研究。
四、展望
近几十年来,人们对肿瘤代谢重编程与表观遗传学修饰的交叉认识和研究取得了重大进展。然而,仍然有许多重要的科学问题有待回答。例如,1)非乙酰化的组蛋白酰化调控,包括丙酰化、丁酰化、巴豆酰化、丙二酰化、2-羟基异丁酰化和戊二酰化等代谢物介导的翻译后修饰,在不同癌症发展中的具体作用和机制是什么?2)当多种翻译后修饰针对同一氨基酸残基(例如,赖氨酸残基)时,不同修饰之间可能存在竞争拮抗,肿瘤细胞如何做到求同存异?3)代谢产物的空间区域化揭示了代谢酶易位在表观遗传学调控中的重要性。因此,发现代谢产物在其他细胞器中的作用,如溶酶体、内质网、高尔基体等,将是理解代谢和表观遗传学如何相互作用以及细胞器互作的关键。4)详尽的解析代谢酶的互作分子及其组装的生物大分子复合物,阐明它们的非代谢(moonlighting)或兼职作用;同时探究代谢物特异结合蛋白,即所谓的“代谢物受体”,对于人们理解和治疗肿瘤将至关重要;5)肿瘤微环境内免疫细胞,菌群、肿瘤细胞与其它细胞在代谢物和表观遗传水平的互作仍然值得长期探索。目前关于表观遗传分子修饰酶如HDAC或DNMT的抑制剂已用于肿瘤治疗,而且代谢酶IDH突变的抑制剂也被FDA批准用于治疗特定的肿瘤。但是,要满足人们日益提高的针对肿瘤的精准治疗和个性化疗法的需求,我们对抗肿瘤之路仍然任重而道远。

原文链接:
https://doi.org/10.1007/s13238-021-00846-7
