——中国科学院上海药物研究所张继稳研究员及其团队
结构决定药品质量,微观结构决胜宏观性质。仿制药能否媲美原研药?创新药如何实现更优制剂?这些是制药产业从“仿制”迈向“创新”必须直面的核心命题。药物制剂并非药物与辅料的简单叠加,而是具备独特精密结构的微观系统,微观尺度下颗粒的堆积方式、孔隙的尺度与分布、界面结合的强弱,共同塑造了制剂内部的复杂微环境,进而决定药物在体内的释放行为与起效节律。尤其是缓控释等复杂制剂,一旦微观结构失控,释放便难以预测,疗效更是无从保障。随着药品审评标准与国际接轨,明晰制剂结构差异及其作用,已不仅是学术探索,更是保障药品质量、确保临床疗效的必由之路。突破传统表征手段局限,将制剂结构转化为可量化、可质控的科学依据,成为行业亟待攻克的关键壁垒。
依托大国重器,领跑结构药剂学
药物制剂体积微小,其内部精细结构研究无法依靠简单的解剖手段。为揭示片剂、微丸、微粒中的微观奥秘,中国科学院上海药物研究所张继稳研究员团队,携手上海光源肖体乔教授等物理学家以及英国Peter York教授团队开展跨学科研究,团队聚焦药物制剂内部精细结构,依托上海光源这一国家重大科技基础设施,系统推进制剂结构的定量研究。

张继稳、Peter York合作指导的第一批结构药剂学博士殷宪振、伍丽与York教授在上海光源讨论实验
这并非一场临时的技术尝鲜,而是一场跨越十六载的科研长跑。自2009年上海光源投入运行之初,张继稳团队便敏锐地捕捉到同步辐射成像技术对药剂学研究的革命性意义,率先推动该技术向制剂领域的应用探索。多年来,团队始终是上海光源面向医药产业领域服务的重要用户,多次承担重点课题,更是全球最早将同步辐射成像技术引入制剂领域的团队之一。
依托大科学装置,充分发挥我国集中力量办大事的制度优势,团队将前沿物理表征手段与药剂学的复杂问题深度融合,提出“结构药剂学”新理论与新方法,并在该交叉研究领域实现全球领跑。
团队的标志性成果之一,是对合肥立方制药股份有限公司创制的高端制剂“非诺地平渗透泵”(立诺®)释药机制的深入揭示。借助同步辐射X射线显微计算机断层成像技术(SR-μCT),研究人员在不同释药阶段对片芯进行无损成像,连续追踪其水化、溶胀及内部结构的动态演变,首次量化了片芯体积、表面积等以往无法测定的关键参数,从微观结构层面揭示了该制剂实现恒速释放的内在机制。这是全球首次运用同步辐射光源成像技术研究渗透泵制剂结构,在此基础上,团队进一步引入分形维度,对片芯内复杂不规则的结构进行定量表征,为控释制剂的内在质量评价开辟了新路径。
敢于挑战“看不见的科学无人区”,团队围绕“结构药剂学”这一重大命题长期深耕、持续攻坚。他们不断打磨研究方法,实现了“见所未见”的突破,将一次次观测发现转化为可复用的研究能力,形成了融合成像技术与定量分析的协同技术路径。基于长期积累,团队进一步提出涵盖剂型结构、制剂中间体微粒结构、制剂体内外动态结构、分子结构的药物制剂四级结构体系,构建起系统的方法论框架。随后,团队将结构研究思路推向一致性评价与产业应用场景,让结构研究服务于药品质量控制与新剂型设计,把制剂结构作为关键抓手,使其成为新药研发和评价的核心依据,将结构、工艺与性能纳入同一逻辑链,清晰解答了“制剂质量该从何处着眼、如何精准判定”的行业难题。凭借卓越的原始创新能力与突出的产业贡献,团队关于结构药剂学及其在高端制剂和药用辅料中的应用研究,荣获2025年中国药学会科学技术奖三等奖与2024年上海市药学会科学技术奖二等奖。
技术突破:从定性观察到定量表征的跨越
制剂结构研究的核心挑战在于其内部结构形态复杂、动态多变,且难以捕捉其演变规律。长期以来,孔隙是否连通、释药通道如何形成、包衣层是否存在隐性缺陷等关键问题,只能依赖溶出曲线间接推断,二维图像或切片观察亦仅能呈现局部信息。
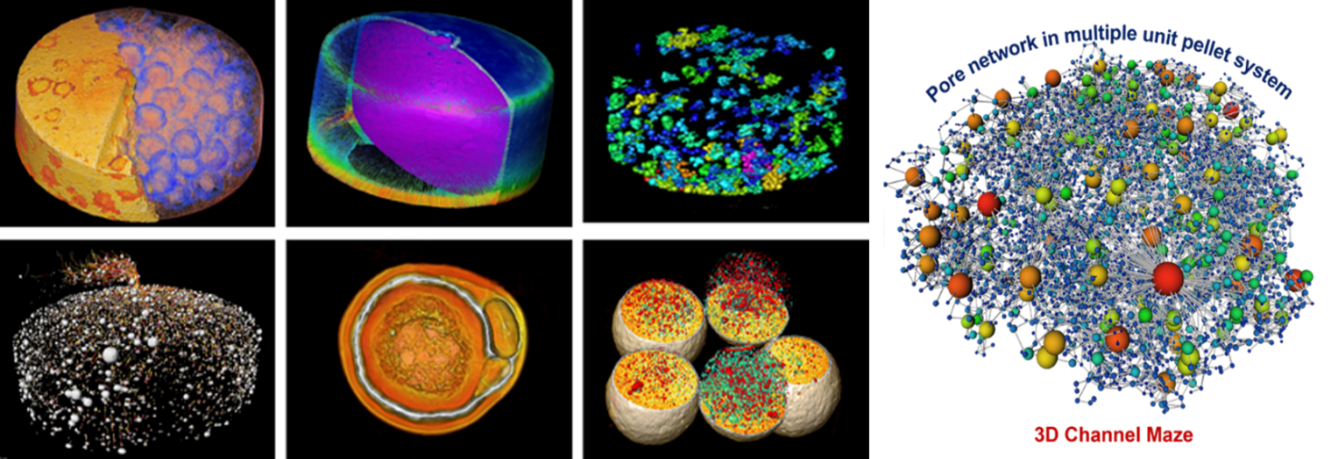
首次应用上海光源揭示的丰富多彩制剂结构
依托上海光源,团队将同步辐射X射线显微计算机断层成像(SR-μCT)、同步辐射红外成像、同步辐射微区X射线衍射等国际领先技术引入制剂结构研究,为破解上述难题提供了全新方案,并率先开展了基于SR-μCT的动态原位成像研究。该技术能够在无破坏条件下,获取制剂内部的三维结构信息,并在微米乃至亚微米尺度进行精确定量分析,部分过程甚至可实现连续观测。由此,制剂内部原本隐匿的结构细节,实现了从定性描述到定量表征的根本性跨越,使得不同制剂间的结构比对与验证成为可能。
更为关键的是,这项技术能力能直接用于研发与评价决策。通过三维结构分析,研究人员既能对比仿制药与原研药的结构一致性,助力反向工程;又能在制剂设计阶段精准研判关键结构是否偏离预期,将质量风险控制从终产品检验阶段前移至处方设计和工艺优化阶段。对于缓控释等复杂固体制剂,三维结构信息还可用于追踪释放通道的形成与演变,将颗粒构型、孔隙网络、界面特性等结构特征,与释药行为、物理稳定性等关键表现建立关联,推动药物制剂研发与评价从依赖经验试错转向基于科学证据的精准判断。
源头创新:从结构认知到结构创造
面对我国药用辅料基础相对薄弱、高端辅料长期面临“卡脖子”风险的现状,张继稳研究员深知唯有源头创新才能掌握产业主动权,而在微粒水平上控制药用辅料、载药微粒的结构特征,正是创新制剂研发的核心所在。团队率先投身环糊精金属有机骨架(CD-MOF)的研究,研发出绿色高效的CD-MOF制备技术,成功创制出立方体、柱状、纳米网格等多种结构的微粒载体,可广泛应用于吸入粉雾剂、缓控释制剂、靶向制剂等领域。
MOF作为重要新型材料,其相关研究于2025年荣获诺贝尔化学奖。张继稳团队在CD-MOF领域的深耕,使我国在MOF的药物应用研究领域跻身国际前沿。围绕这些新型载体,团队不仅致力于构建特定结构的微粒,更深入追踪微粒进入体内后的空间分布与动态命运。借助跨尺度三维成像手段,研究人员能够追踪单个载体颗粒,观察其在组织乃至器官层面的去向与停留情况,让药物递送过程研究摆脱对性能指标的间接推断,获得基于结构证据的直接观察结果。围绕CD-MOF的研究与应用开发,团队设计了吸入粉雾剂、鼻用粉剂、长效注射剂、缓释滴眼剂、高效吸收制剂、靶向制剂等新剂型,在新材料和递送技术上实现全新突破,推动药用辅料的原始创新与转化,成为解决临床用药难题的利器。
仿制药质量和疗效一致性评价是面向全行业的系统工程,国务院办公厅相关文件明确指出,此项工作对保障用药安全有效、提升行业整体水平意义重大。而一致性评价的技术链条长、投入大,从参比制剂选择到工艺验证、生物等效性研究,关键证据的缺失往往会导致返工与不确定性。同时,我国药品批准文号存量庞大,截至2024年底,境内生产药品批准文号达158,336件,境外生产药品批准文号3,252件,此项工作既需提速,又必须经得起长期检验。
张继稳带领团队破解制剂结构认知的难题。尤其是缓控释等复杂制剂,其释放行为的差异往往源于内部微观结构的细微偏差。团队以定量结构为抓手,将三维成像与定量分析相结合,把原本难以厘清的环节转化为可对照、可复核的科学依据,为复杂制剂的一致性研究和逆向工程开发提供了更具操作性的方法路径。
更具深远意义的是,团队正推动“结构药剂学”从结构认知向结构创造跨越。如果说解析传统制剂是“读懂结构”,开发CD-MOF等新型辅料就是“创造结构”;基于鼻腔等人体结构研发鼻用粉雾剂、新型吸入粉雾剂、微粒型缓释滴眼剂等创新制剂,则是“结构转化”。正是基于对药物微观释放机制的深刻理解,团队才能跳出传统辅料的桎梏,自下而上设计出具有特定孔径、特定功能的纳米网格全新超分子载体。这种源于认知、始于设计的创新路径,不仅从根源上破解了高端辅料“卡脖子”的被动局面,更为我国创新制剂的研发构建起完全自主知识产权壁垒。

张继稳研究员在央视“大国重器”专题采访中
“结构是药物和辅料在制剂中存在的形式,也是药品质量监管的新路径。”十六载砥砺前行,张继稳团队在微观世界里构建起一条严密的逻辑链条:以确凿的结构证据取代模糊的经验判断,实现制剂结构的发现与新结构制剂的设计;以自主的源头设计打破被动的技术依赖,以制剂结构研究助力药品质量提升与监管优化。当每一粒国产药都能经得起微观尺度的极致审视,中国医药产业迈向高质量发展的步伐,必将更加从容且坚定。(马烨霞)
