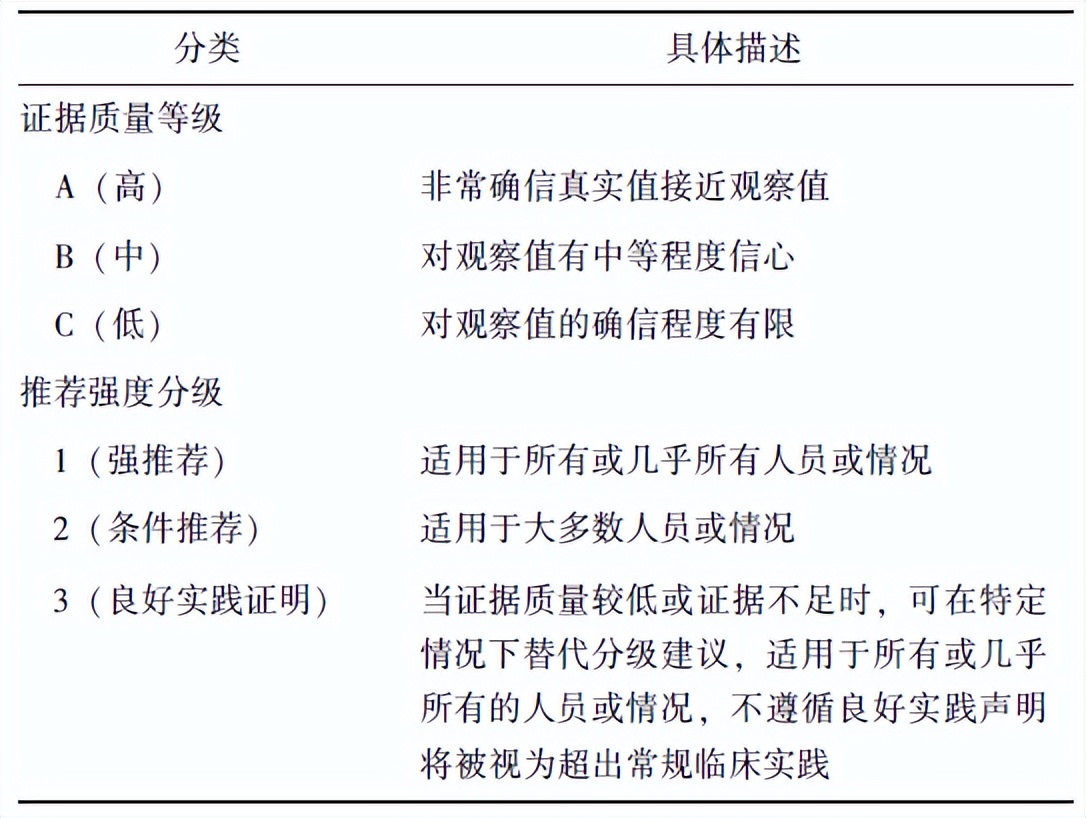
美国甲状腺协会(ATA)于1996年首次发布《甲状腺结节和分化型甲状腺癌诊治指南》,并先后于2006年、2009年和2015年进行了修订。在2025年的最新修订版本中,原指南被拆分为两部分,即《甲状腺结节诊治指南》与《成人分化型甲状腺癌诊治指南》[1]。新版指南所纳入文献的最终检索日期截至2023年10月1日,其循证工作组独立于ATA运作,并采用改良的推荐意见分级评价、制订与评估(GRADE)分级系统对证据质量进行评价(表1)。
表1 GRADE证据质量等级及推荐强度分级表
指南的编写团队涵盖内分泌学、外科学(包括普外科和头颈外科)、核医学、病理学、肿瘤学、癌症遗传学、流行病学及影像学等多个甲状腺癌相关领域的专家。
值得关注的是,本次修订首次引入了1名患者权益代表和1名循证医学专家,旨在全面反映各方观点与需求。本文对主动监测这一热点问题的指南更新要点进行梳理与解读,以期更好地指导主动监测在甲状腺癌管理中的应用。
1主动监测更新要点
1.1 适宜人群
新版指南指出,主动监测是部分低危T1a期甲状腺乳头状癌(PTC)的合理管理策略之一(推荐强度:2C)[2-12]。然而,针对T1b期及以上肿瘤的主动监测,目前证据仍有限,因此未作常规推荐[10,13-15]。在患者选择方面,以下情况被视为不适合主动监测:病理学高危亚型,侵犯喉返神经、气管或食管,明显腺外侵犯,存在淋巴结或远处转移,以及肿瘤靠近后被膜的患者[16-18]。
此外,年龄>60岁的T1a期PTC患者可能更适合接受主动监测。研究表明,与年轻患者(<40岁)相比,该人群发生肿瘤进展(定义为直径增大>3 mm)、新发淋巴结转移或新发临床症状的风险显著降低[19]。值得关注的是,2015版ATA指南并未对主动监测作出正式推荐,仅在第 12 条推荐意见的注释中提及,主动监测可作为以下患者的替代选择:
1低风险 PTC;
2手术风险较高;
3预期生存期较短;
4存在更紧急合并症的患者[20]。
对于主动监测的适宜人群方面,日本、韩国和中国的推荐意见具体如下:
1日本内分泌外科医师学会(JAES)指南[21]:年龄>60岁;穿刺确诊为PTC并排除侵袭性亚型;结节直径≤1.0 cm;无临床可见的淋巴结转移(N0)及远处转移(M0);肿瘤与气管、喉返神经之间存在安全边界(图1);无其他需手术治疗的甲状腺/甲状旁腺疾病(推荐强度:1B)。
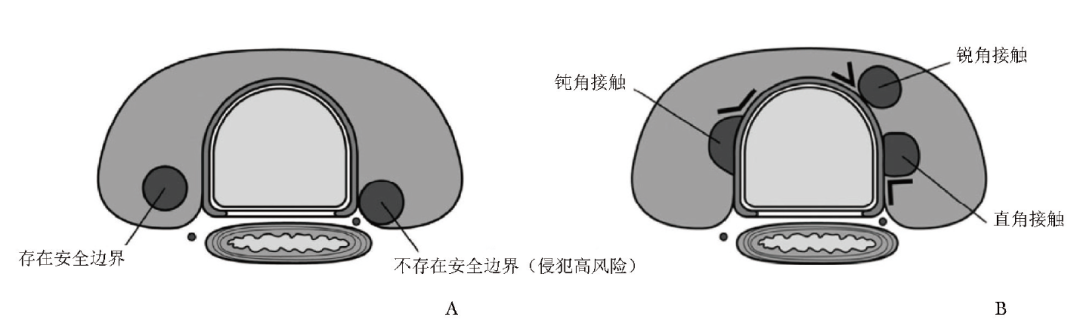
图1 肿瘤与喉返神经(A)和气管(B)的解剖关系示意图[21]
2韩国甲状腺放射协会(KSTR)共识[22]将适宜人群细分为以下两类:①理想人群:单发、T1a期PTC;肿瘤局限于甲状腺实质内,未邻近包膜;无淋巴结或远处转移征象。②适宜人群:虽存在一定随访难度,但在经验丰富的团队管理下仍可考虑主动监测。具体特征包括边界不清的肿瘤、被膜下肿瘤(但无明确侵犯证据)、与气管呈锐角接触等。
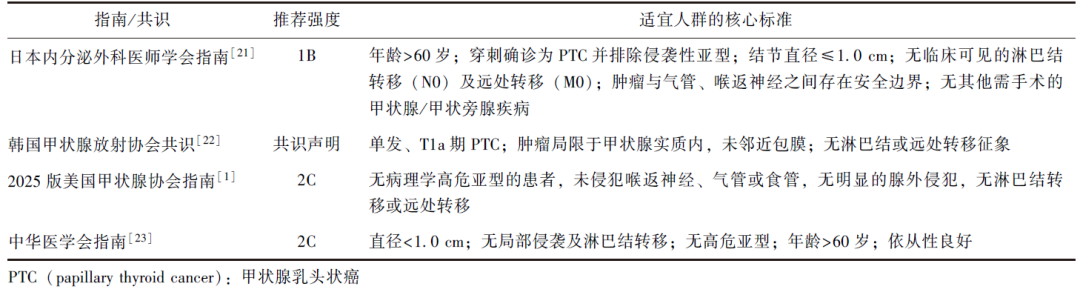
3中华医学会指南[23]:肿瘤直径<1.0 cm;无局部侵袭及颈部淋巴结转移;穿刺未见高危PTC亚型;年龄>60岁;患者依从性良好(推荐强度:3C),详见表2。
表2 各国指南对甲状腺乳头状癌主动监测适宜人群的建议比较
1.2 监测方法
新版指南建议,在主动监测期间应每 6~12个月通过颈部超声评估疾病进展(推荐强度:3C)[9,19,24],但不推荐常规监测甲状腺球蛋白(Tg)与抗甲状腺球蛋白抗体(TgAb)(推荐强度:2C)。在临床实践中,可采取在主动监测的前1~2年内每6个月进行1次颈部超声检查,之后若病情稳定可调整为每年监测1次。
然而,关于主动监测应在何时终止,目前尚无明确结论[24]。日本、韩国的指南在随访频率上与此基本一致,均建议在前2年每半年复查1次超声,若2年后肿瘤保持稳定,则可改为每年1次。此外,韩国指南特别强调了对肿瘤形态的细致评估,建议分别测量肿瘤的横径、纵径和前后径,并以其中最大值作为判断依据(图2)。
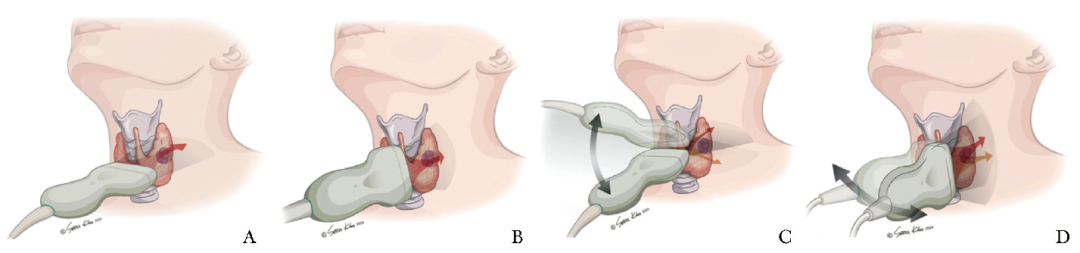
图2 甲状腺结节超声测量标准平面示意图[22]
A.横断面;B.矢状面;C.于横断面通过探头角度<45°测量最大肿瘤前后径;D.于矢状面通过探头角度<45°测量最大肿瘤前后径
1.3 手术指征
新版指南指出,对于正在接受主动监测的患者,以下情况应考虑终止监测并接受手术切除:
1发现经活检证实的新发淋巴结转移;
2原发肿瘤直径增长≥3 mm;
3出现远处转移;
4存在腺外侵犯;
5肿瘤向后侧被膜生长(可能威胁气管或喉返神经);
6患者因过度焦虑或主观意愿要求手术(推荐强度:3)。
日本指南中终止主动监测的指征包括:
1肿瘤直径达到13 mm;
2出现新发淋巴结转移;
3患者意愿改变,要求手术。
4出现需要手术治疗的其他甲状腺或甲状旁腺疾病。
韩国指南中提出的终止标准为:
1当T1a期PTC增长至13 mm(或两个维度达到 12 mm);
2出现新发淋巴结转移;
3患者观念或偏好发生改变;
4发现需手术治疗的甲状腺或甲状旁腺疾病。
需特别说明的是,日本指南认为肿瘤侵犯前被膜及带状肌并非立即手术的绝对指征,可在必要时再行切除手术;而美国和韩国指南则将其视为应终止监测并立即手术的明确指征。
2小结
近年来,主动监测已成为分化型甲状腺癌领域医患共同关注的热点,同时也引发了广泛的学术讨论。自1993年日本KUMA医院Ito医生首次提出对微小低危分化型甲状腺癌采取主动监测以替代手术以来,该策略逐渐受到重视[25-26]。2023年7月,该医院发表的30年随访结果显示[27],对低危分化型甲状腺癌患者实施主动监测与立即手术在远期肿瘤学结局方面无统计学差异,进一步支持了该策略的可行性。在国内,程若川团队基于对PTC患者25个月的主动监测结果指出,该策略同样适用于中国人群[28]。
然而,一项基于SEER数据库的研究提出了不同结论,发现延期手术超过180 d的患者其甲状腺癌特异性死亡风险较90 d内接受手术者升高约4倍[29]。尽管目前多数国际指南对主动监测给予了一定程度的推荐,其在我国临床实践中的推广仍面临诸多挑战与争议:(1)适应证尚未统一,国内相关研究中符合日本KUMA医院标准的患者占比达72.6%,而符合中国共识标准者仅为14.4%;(2)缺乏统一的标准化操作流程,主动监测并非等同于“躺平式监测”;(3)“带瘤生存”理念与中国患者的传统健康观念存在冲突,易引发焦虑情绪,影响依从性;(4)我国甲状腺专科医师数量不足,各地区、医疗机构对主动监测的理解与应用存在差异,难以实现密切、规范及专业的随访管理。
除肿瘤学结局外,Hedman等[30]研究发现,虽然甲状腺癌进展相对缓慢,但其引发的焦虑情绪在术后15年仍可持续存在。约48%的患者因担忧复发而产生焦虑情绪;而选择主动监测的患者,其焦虑程度甚至高于手术患者,尤其在监测初期,因无法预判肿瘤进展,担心出现淋巴结或远处转移,焦虑症状更为显著。
2025版ATA指南的发布,为主动监测的临床实践提供了系统、权威的指导,也为中国相关指南的更新提供了重要参考。随着更多高质量研究的推进,主动监测在甲状腺癌管理中的应用有望得到进一步规范与推广。
(本文编辑:李慧文)

